Hauptmerkmale:
- Ready to use: Reagenzien als kompletter Mastermix pre-aliquotiert und gebrauchsfertig in 8-Well-Streifen. Die Teststreifen können bei Raumtemperatur gelagert werden.
- Easy to use: Kein Einfrieren, Auftauen oder Pipettieren auf Eis erforderlich. Die wenigen verbleibenden Schritte minimieren das Risiko von Fehlern oder Kontaminationen.
- Hohe Sensitivität: LOD bis zu 0,5%
- Große Flexibilität: Für geringe Mengen an DNA oder RNA aus verschiedenen Quellen, wie z.B. FFPE und Plasma.
- Schnell: Vom Gewebe zum Ergebnis in weniger als 3 Stunden mit einer Hands on Time < 10 Minuten.
- Qualität: hergestellt nach ISO 13485
- Zertifikation: Die Kits wurden in Übereinstimmung mit der Richtlinie 98/79/EG über In-vitro-Diagnostika (IVD) konzipiert, entwickelt und validiert.
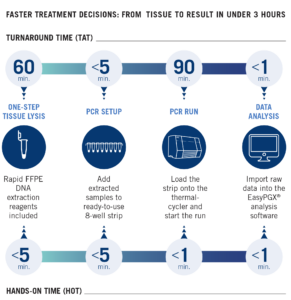
Workflow System EasyPGX: vom Gewebe zum Resultat in weniger als 3 Stunden.
Merkmale
Nachweis der wichtigsten Mutationen von Exon 2 (Codone 12, 13), Exon 3 (Codone 59, 61) und Exon 4 (Codone 117, 146) des KRAS-Gens mittels 8 Mischungen aus Oligonuklotiden. Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens.
Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität der in den Proben vorhandenen DNA.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Sensitivität
Das Kit ermöglicht den Nachweis von geringen Anteilen an mutierten Allelen bei großen Mengen an genomischer DNA Wild-Typ durch Real-Time-Amplifikation mit spezifischen Sequenz-Sonden, die mit FAM und HEX markiert sind. LOD bis zu 0,5%.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA, die aus Gewebe (frisch, gefroren, FFPE) oder Plasma * extrahiert wurden.
*Reagenzien, Verbrauchsmaterialien und Zubehör für die Extraktion aus Plasma sind separat erhältlich (siehe Linie Helix, Code H8040).
Merkmale
Nachweis der wichtigsten Mutationen des Codons 600 des BRAF-Gens mittels 4 Mischungen aus Oligonuklotiden.
Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens.
Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität der in den Proben vorhandenen DNA.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Sensitivität
Das Kit ermöglicht den Nachweis von geringen Anteilen an mutierten Allelen bei großen Mengen an genomischer DNA Wild-Typ durch Real-Time-Amplifikation mit spezifischen Sequenz-Sonden, die mit FAM und HEX markiert sind. LOD bis zu 0,5%.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA, die aus Gewebe (frisch, gefroren, FFPE) oder Plasma * extrahiert wurden.
*Verbrauchsmaterialien und Zubehör für die Extraktion aus Plasma sind separat erhältlich (siehe Linie Helix, Code H8040)).
Merkmale
Nachweis der wichtigsten Mutationen, Insertionen und Deletionen der Exons 18, 19, 20 und 21 des EGFR-Gens mittels 8 Mischungen aus Oligonuklotiden.
Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens.
Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität der in den Proben vorhandenen DNA.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Sensitivität
Das Kit ermöglicht den Nachweis von geringen Anteilen an mutierten Allelen bei großen Mengen an genomischer DNA Wild-Typ durch Real-Time-Amplifikation mit spezifischen Sequenz-Sonden, die mit FAM und HEX markiert sind. LOD bis zu 0,5%.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA, die aus Gewebe (frisch, gefroren, FFPE) oder Plasma * extrahiert wurden.
*Reagenzien, Verbrauchsmaterialien und Zubehör für die Extraktion aus Plasma sind separat erhältlich (siehe Linie Helix, Code H8040).
Merkmale
Nachweis der wichtigsten Mutationen von Exon 2 (Codone 12, 13), Exon 3 (Codone 59, 61) und Exon 4 (Codone 117, 146) des NRAS-Gens mittels 8 Mischungen aus Oligonuklotiden. Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens. Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität der in den Proben vorhandenen DNA.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Sensitivität
Das Kit ermöglicht den Nachweis von geringen Anteilen an mutierten Allelen bei großen Mengen an genomischer DNA Wild-Typ durch Real-Time-Amplifikation mit spezifischen Sequenz-Sonden, die mit FAM und HEX markiert sind. LOD bis zu 0,5%.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA, die aus Gewebe (frisch, gefroren, FFPE) oder Plasma * extrahiert wurden.
*Reagenzien, Verbrauchsmaterialien und Zubehör für die Extraktion aus Plasma sind separat erhältlich (siehe Linie Helix, codice H8040)
Merkmale
Nachweis der wichtigsten chromosomalen Translokationen, an denen die Gene ALK, ROS1, RET und das Skipping von Exon 14 beim MET-Gen beteiligt sind. OJeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Fusionen sowie eines endogenen Kontrollgens.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer RNA/DNA-Sequenzen enthält, die den wichtigsten, durch das Kit nachgewiesenen Fusionen entsprechen.
- Negativkontrolle.
Ausgangsmaterial
RNA aus Gewebeproben (frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE)) oder zytologischen Proben.
Merkmale
Nachweis durch allelische Diskriminierung der vier Polymorphismen von DPYD*2A (IVS14+1G>A, c.1905+1G>A, rs3918290), DPYD*13 (c.1679T>G, rs55886062), DPYD D949V (c.2846A>T, rs67376798) und DPYD IVS10 (c.1129– 5923C>G, rs75017182) des DPYD-Gens, die mit der Toxizität aufgrund einer Behandlung mit Fluoropyrimidinen verbunden sind, mittels 4 Mischungen aus Oligonuklotiden. Jeder Mix aus Oligonuklotiden ermöglicht die Co-Amplifikation der mutierten (FAM) und der Wild-Type (HEX) Sequenzen.
Kontrollen
- DPYD WT Positivkontrolle: enthält eine Mischung aus synthetischer DNA Wild-Type für alle analysierten DPYP-Polymorphismen.
- DPYD MT Positivkontrolle: enthält eine Mischung aus synthetischer mutierter DNA für alle analysierten DPYP-Polymorphismen.
- Negativkontrolle.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von genomischer DNA, die aus Vollblut extrahiert wurde.
Merkmale
Nachweis durch allelische Diskriminierung der Polymorphismen UGT1A1*1 (TA)6, UGT1A1*28 (TA)7, UGT1A1*36 (TA)5 und UGT1A1*37 (TA)8 in der Promotorregion des UGT1A1-Gens, die mit einer Toxizität aufgrund einer Behandlung mit Irinotecan verbunden sind, mittels einer einzigen Mischung aus Oligonuklotiden. Der Mix UGT1A1 enthält mit HEX markierte Sonden zum Nachweis von UGT1A1*28 und UGT1A1*37 sowie mit FAM markierte Sonden zum Nachweis von UGT1A1*1 und UGT1A1*36.
Kontrollen
- UGT1A1 WT Positivkontrolle: Positive Amplifikationskontrolle, die synthetische DNA mit mutiertem Genotyp UGT1A1*1/*1 enthält.
- UGT1A1 MT Positivkontrolle: Positive Amplifikationskontrolle, die synthetische DNA mit mutiertem Genotyp UGT1A1*28/*28 enthält.
- Negativkontrolle.
Ausgangsmaterial
Die Kits ermöglichen die Analyse von genomischer DNA, die aus Vollblut extrahiert wurde.
Merkmale
Nachweis der wichtigsten Mutationen von Exon 2 (Codone 12,13), Exon 3 (Codon 61) der Gene KRAS, NRAS, HRAS sowie der Codone 600 und 601 des BRAF-Gens. Jeder Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer RNA/DNA-Sequenzen enthält, die den wichtigsten, durch das Kit nachgewiesenen Fusionen entsprechen.
- Negativkontrolle.
Ausgangsmaterial
DNA aus Gewebeproben (frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE)) oder zytologischen Proben.
Merkmale
Quantitative Bestimmung von DNA-Fragmenten größer als 200 bp. Die Kombination aus iFOBT und quantitativer Analyse der aus dem Stuhl extrahierten DNA ist ein nützliches Instrument, um die Früherkennung von CRC zu verbessern und die Wahrscheinlichkeit des Vorhandenseins von CRC abzuschätzen.
Kontrollen
- Positivkontrolle, genomische DNA in bekannter Konzentration;
- Standard, genomische DNA in bekannter Konzentration, die zur Erstellung der Standardkurve verdünnt wird;
- Spike, Kontroll-DNA, die den Proben zur Überprüfung der Hemmung zugesetzt wird;
- Negativkontrolle.
Ausgangsmaterial
DNA aus Stuhl.
Merkmale
Das einzige komplette Kit für die In-vitro-Diagnostik, das den Nachweis der Mutationen T790M und C797S (2 Varianten) des EGFR-Onkogens durch Real-Time PCR ermöglicht. Die T790M-Mutation stellt sowohl den Hauptmechanismus der erworbenen Resistenz gegen EGFR-Tyrosinkinase-Inhibitoren der ersten und zweiten Generation dar, als auch das Ziel von EGFR-TKI der dritten Generation. Während die C797S-Mutation in zahlreichen Studien als einer der Faktoren identifiziert wurde, die für die Resistenz gegen letztere Arzneimittel verantwortlich sind.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA, die aus Gewebe (frisch, gefroren, FFPE) oder Plasma * extrahiert wurden.
*Reagenzien, Verbrauchsmaterialien und Zubehör für die Extraktionaus Plasma sind separat erhältlich (siehe Linie Helix, Code H8040)).
Merkmale
Nachweis der wichtigsten Mutationen des IDH1-Gens (Codone 105, 132) und des IDH2-Gens (Codone 140, 172). Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Allele sowie eines endogenen Kontrollgens. Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität der in den Proben vorhandenen DNA.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Ausgangsmaterial
DNA aus Gewebeproben: frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE).
Merkmale
Nachweis der chromosomalen Translokationen an denen die Gene RET/PTC1 beteiligt sind: CCDC6-RET; RET/PTC2: PRKAR1A-RET; RET/PTC3: NCOA4-RET und PAX8/PPARG. Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation eines oder mehrerer mutierter Fusionen sowie eines endogenen Kontrollgens.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer RNA/DNA-Sequenzen enthält, die den wichtigsten, durch das Kit nachgewiesenen Fusionen entsprechen.
- Negativkontrolle.
Ausgangsmaterial
RNA aus Gewebeproben (frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE)) oder zytologischen Proben.
Merkmale
Nachweis von 8 „quasi-monomorphen“ Mononukleotidmarkern: BAT-25, BAT-26, NR-21, NR-22, NR-24, NR-27, CAT-25 und MONO-27 durch Real Time PCR und anschließender Analyse der Targets mithilfe einer Denaturierungskurve. Der Test ermöglicht einen präzisen und schnellen Nachweis von Mikrosatelliten-Instabilität in Tumorproben.
Kontrollen
- Positivkontrolle, genomische DNA, die einem stabilen Profil entspricht
- Negativkontrolle.
Ausgangsmaterial
DNA aus Gewebeproben: frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE). Ein paralleler Abgleich mit normalem Gewebe oder Blut ist nicht erforderlich.
Merkmale
Identifikation der 14 Hochrisiko-Genotypen (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66 und 68) der humane Papillomaviren (HPV) durch Amplifikation der Onkogene E6 und E7. Jeder Mix ermöglicht die Co-Amplifikation der HPV-Typen sowie eines endogenen Kontrollgens mit Genotyp spezifischen Sonden.
Ausgangsmaterial
DNA aus Zervixabstrichen und aus in formalinfixierten und in Paraffin eingebettet Gewebeproben (FFPE).
Merkmale
Nachweis von Fusionsvarianten der Gene NTRK1, NTRK2 und NTRK3 durch One Step Real Time. Der Test ermöglicht den Nachweis der vom Kit identifizierten Genumlagerungen unter Verwendung von Primern und Sonden, die es ermöglichen, die vom Kit analysierten Fusionen im FAM-Kanal selektiv zu amplifizieren.
Kontrollen
- Kontrolltest: Test zur Bestimmung des DNA-Gehalts in der Probe. Zusätzlich wird in jeder Mischung ein endogenes Kontrollgen nachgewiesen, das es ermöglicht die korrekte Durchführung des Amplifikationsverfahrens und das mögliche Vorhandensein von Inhibitoren, die zu falsch-negativen Ergebnissen führen könnten, zu überprüfen.
- Positivkontrolle: enthält eine Mischung synthetischer DNA-Sequenzen, die jeder durch das Kit nachgewiesenen Mutation und genomischer DNA Wild-Type entsprechen;
- Negativkontrolle.
Ausgangsmaterial
Isolierte RNA aus Gewebeproben (frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE)) oder zytologischen Proben.
Merkmale
Nachweis der wichtigsten Mutationen des PIK3CA-Gens (Codone 345, 420, 542, 545, 546, 1047 und 1049).
Kontrollen
- Kontrolltest: Test zur Bestimmung des DNA-Gehalts in der Probe. Zusätzlich wird in jeder Mischung ein endogenes Kontrollgen nachgewiesen, das es ermöglicht die korrekte Durchführung des Amplifikationsverfahrens und das mögliche Vorhandensein von Inhibitoren, die zu falsch-negativen Ergebnissen führen könnten, zu überprüfen.
- Controllo positivo: contiene una miscela di sequenze di DNA sintetico che corrispondono ad ogni mutazione rilevata dal kit e di DNA genomico wild-type;
- Negativkontrolle.
Ausgangsmaterial
Isolierte genomische DNA aus Gewebeproben (frisch, gefroren, formalinfixiert und in Paraffin eingebettet (FFPE)) oder Plasma.*.
* Reagenzien, Verbrauchsmaterialien und Zubehör für die Extraktion aus Plasma sind separat erhältlich (siehe Linie Helix, Code H8040).
Das ‚EasyPGX® ready Lung Fast Track‘-Kit ist ein In-vitro-Diagnosetest für den qualitativen Nachweis der wichtigsten somatischen Mutationen in BRAF (Codon 600), KRAS (Codon 12) und EGFR (Exons 19, 20) mittels Real-Time-PCR, 21) in genomischer DNA, die aus in Formalin fixiertem, in Paraffin eingebettetem Tumorgewebe (FFPE) oder aus zirkulierender Tumor-DNA (ctDNA) isoliert wurde, die aus EDTA-Vollblutplasma von Patienten mit nicht-kleinzelligem Lungenkrebs (NSCLC) gewonnen wurde; NSCLC).
Der Test soll Kliniker bei der Identifizierung von Patienten mit NSCLC-Lungenkrebs unterstützen, die für eine Behandlung mit EGFR-Tyrosinkinase-Inhibitoren, KRAS-Inhibitoren und BRAF-Inhibitoren in Frage kommen, basierend auf dem Mutationsstatus der EGFR-, KRAS- bzw. BRAF-Gene.
Merkmale
Nachweis der häufigsten FGFR3-Genmutationen in den Exons 7, 9, 14, und FGFR2, FGFR3-Genfusionen durch 8 Mischungen von Oligonukleotiden.
Jeder Oligonuklotid-Mix ermöglicht die Co-Amplifikation des Targets sowie eines endogenen Kontrollgens.
Ein spezifischer Mix an Kontrolloligonukleotiden ermöglicht die Bewertung der Qualität und Quantität jeder Probe.
Kontrollen
- Positivkontrolle, die eine Mischung synthetischer Wild-Type DNA-Sequenzen enthält, die jeder durch das Kit nachgewiesenen Variante in einen Background an DNA und RNA Wild-Type entsprechen;
- Negativkontrolle
Sensitivität
Das Kit weist eine Spezifizität von 100% und eine Sensibilität von über 97% auf.
Ausgangsmaterial
Das Kit ermöglicht die Analyse von DNA und RNA, die aus Tumorgewebe (frisch, gefroren bzw. Formalin-fixiert Paraffin-eingebettet (FFPE)) extrahiert wurden.

Eine oder mehrere Broschüren auswählen und zum Herunterladen bitte Ihre Daten angeben
Category
Realtime PCR




